每天早上,闹钟一响,灵魂还在被窝里流连忘返,身体却已被迫上线。顺手倒一杯温水,吞下几片维生素,对不少打工人来说,这一整套流程无异于给「打工模式」做预热。它未必能立刻让人精神焕发,却多少带着一点「我已经在为健康努力了」的仪式感。
不过,也并非所有人都信奉这种「瓶瓶罐罐大法」,有人更愿意把希望寄托在「肉、谷物、蔬菜和坚果」营养均衡的一日三餐中。在他们看来,只要搭配得当,日常饮食本身就蕴藏着支撑身体高效运转的营养分子,足以为忙碌的一天提供稳定而持久的能量基础。
维生素B6充足,免疫不掉线
近期,来自清华大学的研究团队发表于Cell子刊Developmental Cell的一项研究就为我们展示了维生素B6这种存在感不算强,却几乎无处不在的水溶性B族维生素的另一种「高光时刻」。
这项研究发现,通过日常饮食摄入的维生素B6及其活性形式磷酸吡哆醛(PLP),不仅参与基础代谢,更能深度影响免疫系统的工作方式,它能帮助CD8⁺ T细胞维持一种更「年轻」、更持久的状态,使其在对抗肿瘤时不易疲劳,持续输出战斗力。

维生素B6看起来并不起眼,实际上忙得不可开交。它参与氨基酸代谢、神经递质合成等一系列生理过程,平时就藏在肉类、全谷物、蔬菜和坚果中,几乎每天都会和我们打照面。正是这样一种看似普通的营养素,却在悄悄支撑着免疫系统的正常运转。
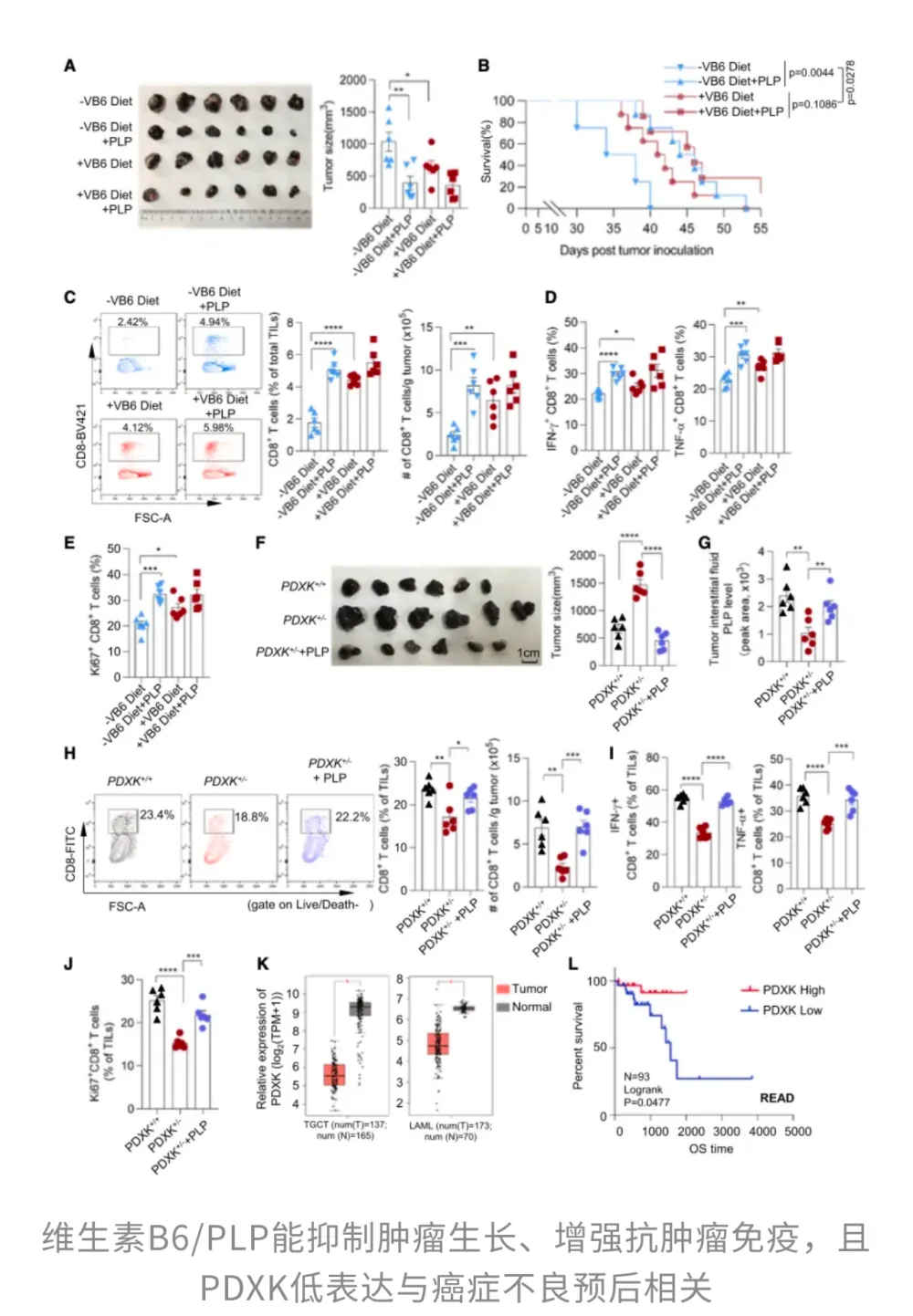
研究团队在黑色素瘤小鼠模型中发现,相较于摄入的饮食中缺乏维生素B6的小鼠,摄入正常含量维生素B6的小鼠体内肿瘤明显更小。与此同时,肿瘤中的CD8⁺ T细胞数量也随之增加,这些免疫细胞不仅增殖更积极,还能分泌更多具有杀伤力的细胞因子(比如IFN-γ和TNF-α)。
不过,并不是任意一种形式的维生素B6都能有效抑制肿瘤,真正发挥作用的是它的活性形式——酸吡哆醛(PLP)。在肺转移模型中,只有补充PLP,才能明显减少转移灶,延长小鼠生存时间。即便是在早期缺乏维生素B6的情况下,在肿瘤形成后补充PLP,依然能够在一定程度上「亡羊补牢」,让CD8⁺ T细胞数量回升,抗肿瘤能力重新上线。
这意味着,PLP不仅可以防患于未然,还能在「敌后」展开救援,「训练」免疫细胞,让它们在抗肿瘤战场上更持久、更高效。
PLP让T细胞更「耐造」
那么,这种关键分子从哪里来呢?这便要归功于合成PLP的关键酶吡哆醛激酶(PDXK)了。它就像PLP的「生产车间」,负责把普通维生素B6转化成战斗力满满的PLP。当PDXK功能受损时,体内PLP水平随之下降,肿瘤生长速度加快,CD8⁺ T细胞的数量和功能也同步下滑。但补充PLP后,这些不利情况能够被恢复。
这条通路在人类肿瘤中同样存在重要意义。正常组织中PDXK表达较高,而在部分肿瘤(如急性髓系白血病)中明显下降。结直肠癌患者中,PDXK表达越低,生存率越低。
也就是说,通过转化为PLP,维生素B6能够帮助CD8⁺ T细胞保持「年轻态」,增强持久作战能力,从而有效抑制肿瘤生长。
T细胞的这种「年轻态」,在免疫学上被称为「干性」。简单来说,CD8⁺ T细胞原本是击杀癌细胞的「战士」,但长期处在高压的肿瘤微环境中,它们很容易被「耗竭」,无法增殖,功能逐渐衰退,最终对癌细胞「缴械投降」。不过,总有一小撮T细胞特别「扛造」,它们保留着类似干细胞的特性,能自我更新,长期持久作战。
那么,PLP究竟给这些T细胞施了什么「魔法」,让它们得以保持这种「年轻态」?研究团队进一步分析后发现,接受PLP处理的T细胞,其表面代表「年轻态」的标志物(如CD62L、TCF1)表达水平明显升高,而代表「耗竭态」的标志物(如PD-1、TIM3)表达水平明显下降。
由此可见,PLP并不是简单地让T细胞变得更亢奋,而是将它们维持在一种更具潜力、更不容易耗竭的干细胞样状态。换句话说,PLP让这些「免疫战士」既能持久作战,又不轻易「累瘫」,为抗肿瘤提供了更可靠的内在支撑。

给BACH2穿上「防护甲」
让干性不再轻易流失
于是,研究者通过代谢组学分析继续抽丝剥茧,他们很快发现,PLP改变的不只是免疫表型,更是T细胞的「内在运行模式」。在PLP的作用下,T细胞的能量供应方式发生了明显转向。原本,它们更偏爱「来也匆匆,去也匆匆」的糖酵解通路;而现在,则逐渐转向依赖线粒体氧化这种更稳定、耐力更强的能量模式。
两种代谢策略,几乎对应着两种截然不同的命运:前者更像爆发力强的短跑选手,效应T细胞比较「短命」,容易耗竭;后者更像节奏稳定的「马拉松选手」,更有利于形成持久、具有记忆特征的T细胞。
这说明,PLP并不是让T细胞更「拼命」,而是教会它们「把能量花在刀刃上」,用更「经济」、高效的方式,撑起一条更长久的免疫防线。
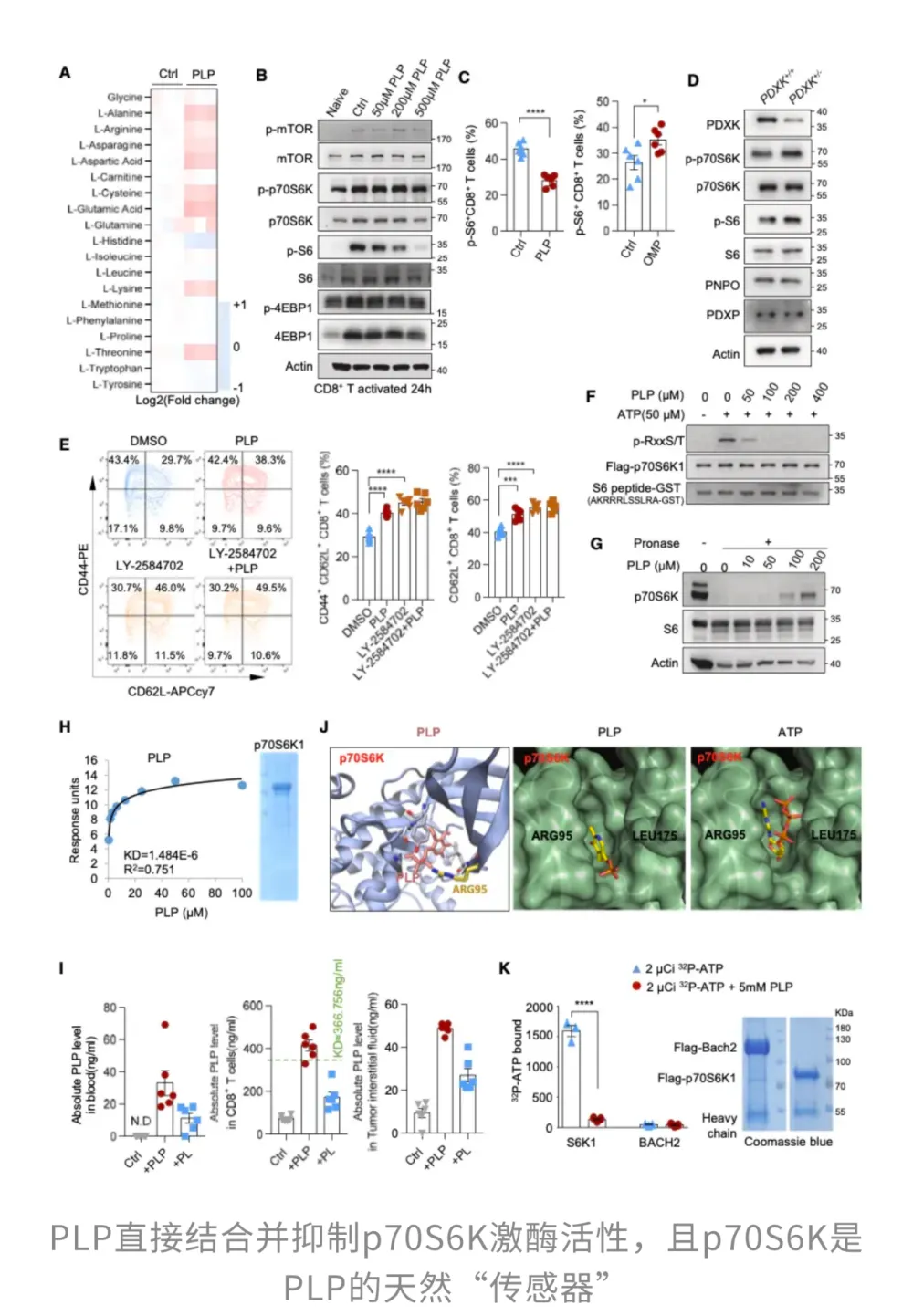
那么,这种「节能模式」究竟是怎么被打开的?顺着信号通路往下追溯,研究者锁定了p70核糖体蛋白S6激酶(p70S6K)。作为mTOR通路下游的重要节点,它通常负责推动细胞生长、增殖和蛋白合成。而p70S6K发挥作用的方式,也相当直接:它通过磷酸化下游的S6蛋白,把细胞推入高代谢、高输出的工作状态。
正是在这个关键节点上,PLP有了「用武之地」。在PLP存在的情况下,CD8⁺ T细胞中 S6的磷酸化水平明显下降;而一旦通过抑制PDXK阻断PLP的生成,p70S6K便迅速「满血复活」,S6再次被大量磷酸化,T细胞也随之更快地滑向高消耗、易耗竭的轨道。
综合来看,PLP通过精准抑制p70S6K这一关键节点,避免CD8⁺ T细胞被推入高代谢、高消耗的「疲劳」轨道,让它们在保持功能性的同时,也具备更强的持久性和可塑性。免疫系统,也因此从「拼体力」,升级为「讲策略」。
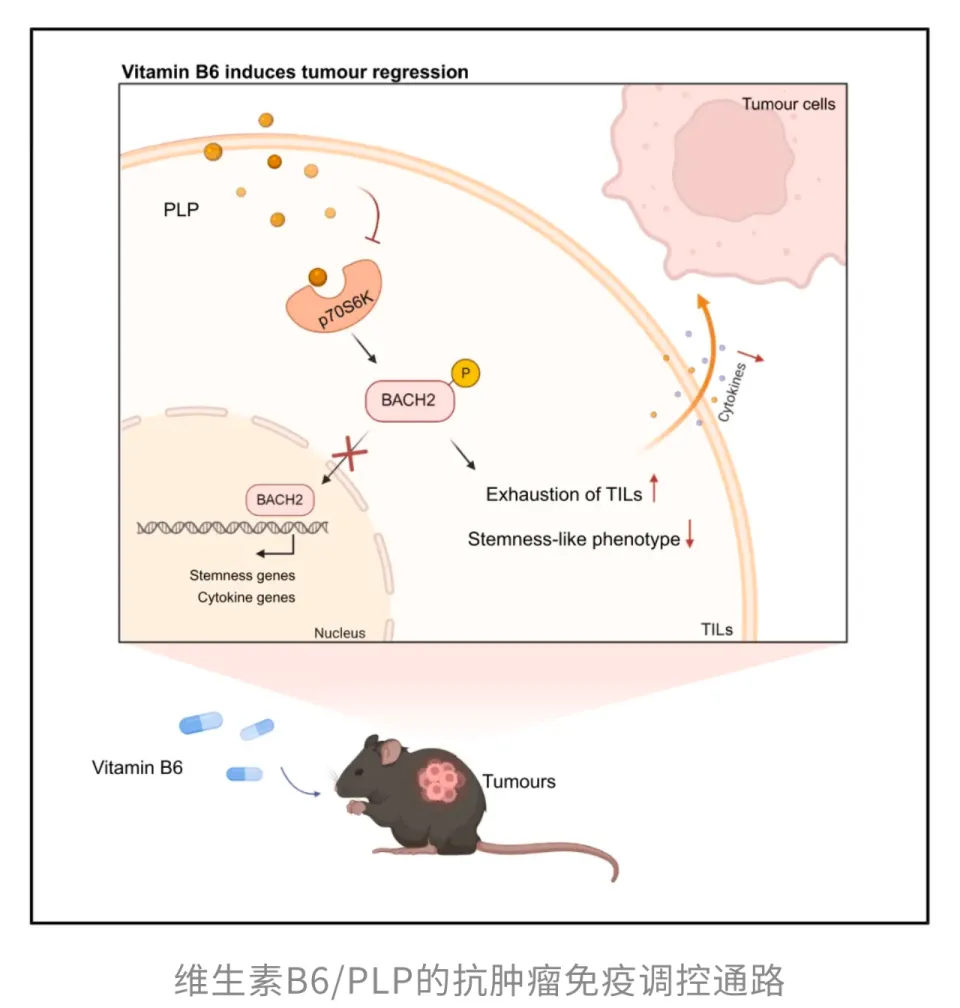
除了代谢这一宏观调控,PLP还调控着T细胞内部的「微观开关」——转录因子BACH2。平时,p70S6K会在BACH2的S520位点打上磷酸化标签,把它「请出」细胞核,使其无法继续控制干性基因,这就好比让T细胞失去了保护膜,容易迅速耗竭。而PLP却像给细胞贴上了一层保护膜,阻止这一磷酸化发生,让BACH2稳稳滞留在核内,持续激活干性基因,同时压低耗竭相关信号。这样一来,T细胞既能保持战斗力,又能持久作战,不至于「熬不住」。
当然,这项研究还极具临床转化价值。在黑色素瘤小鼠模型中,研究者将PLP与一种常用的免疫检查点抑制剂抗PD-1抗体联合使用。结果显示,这两者的组合产生了明显的协同效应,不仅比单独使用PLP或抗PD-1更有效地抑制肿瘤生长,还显著延长了小鼠的生存期,甚至有部分小鼠达到了完全缓解的效果。
这么说,PLP不仅能够单独优化T细胞功能,还能与现有免疫疗法形成互补,使抗肿瘤免疫的「火力」更持久、更强大。
总的来说,这项研究揭示了,维生素B6的活性形式PLP就像给T细胞加了一道「保护屏障」。它能直接抑制激酶p70S6K,让BACH2避免被「打磷酸化标签」而离开细胞核。于是,BACH2稳稳留在核内,持续激活干性相关基因,同时压下那些让T细胞快速「疲劳」的耗竭基因,最终提升它们的抗肿瘤免疫功能。
研究也给我们提了个醒,鸡肉、猪瘦肉、三文鱼、菠菜、土豆、开心果和葵花籽等这些随处可见的「老面孔」,除了能让我们「填饱肚子」,满足味蕾,它们所富含的维生素B6,在体内经过一系列精巧的转化后,竟还能为抵抗肿瘤的「持久战」储备耐力,可以说「浑身是宝」了~
注:上述研究主要基于小鼠模型,尽管临床前数据支持维生素B6的抑瘤作用,其实际临床疗效仍需未来临床试验进一步验证。
参考资料:
Wu J, Li G, Zhou J, Sun X, Wang H, Gong H, Jiang P. Vitamin B6 preserves the stemness-like phenotypes and antitumor ability of CD8+T cells. Dev Cell. 2025 Nov 27:S1534-5807(25)00691-4. doi: 10.1016/j.devcel.2025.10.017. Epub ahead of print. PMID: 41314217.